Las principales propiedades del dióxido de azufre son: Densidad: 2,63 kg/m 3. Masa molar: 64,066 g/mol. Punto de fusión: -72 °C. Punto de ebullición: -10 °C. Obtención del dióxido de azufre. Los métodos de obtención de azufre son: Combustión del azufre y del sulfuro de hidrógeno: S 8 + 8 O 2 » 8 SO 2 2 H 2 S + 3 O 2 » 2 H 2 O + 2 SO 2.. Propiedades físicas del Azufre. Las propiedades físicas del azufre incluyen su color amarillo característico, el olor distintivo y su baja solubilidad en agua. Es un material no metálico con una densidad relativamente baja y puntos de fusión y ebullición específicos que lo hacen notable en el ámbito científico y en aplicaciones prácticas.

Propiedades químicas del azufre. Caracterización y punto de ebullición del azufre

Obtención de distintas formas de azufre elemental QUIMICLAN
Ciclo del Azufre YouTube

El azufre se calienta en un tubo de ebullición. El azufre se funde a una temperatura de 118.85
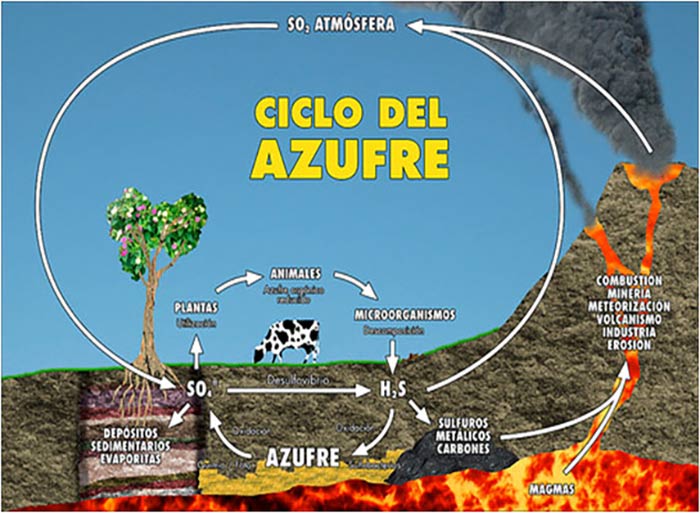
¿Cuál es el ciclo del azufre o ciclo biogeoquímico del azufre? ️ GT

Punto de ebullición, método Siwoloboff YouTube
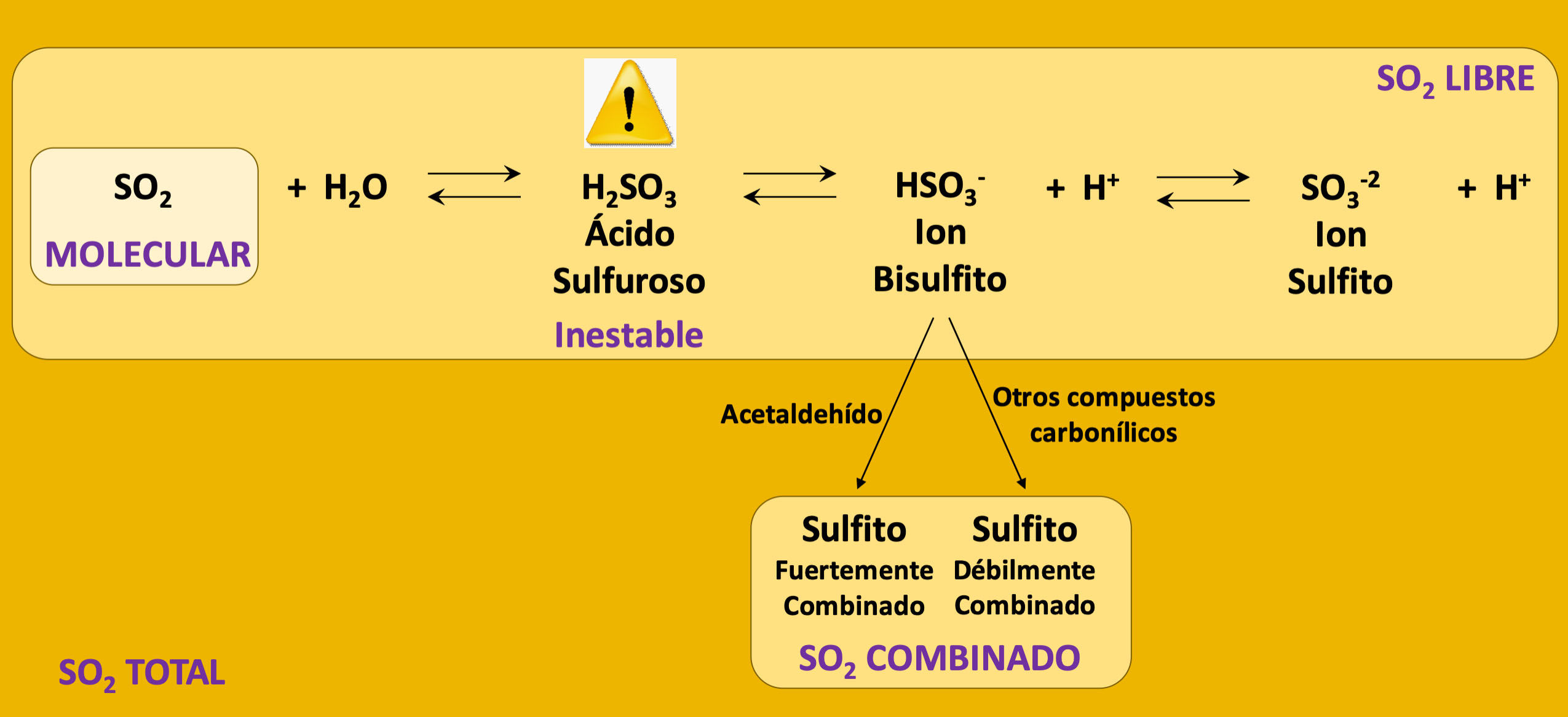
Química del dióxido de azufre en el vino Web oficial TDI

Punto de ebullición Enciclopedia de Energia
![Ciclo del Azufre [ Características ] Etapas e Importancia en 2022 Trucos para la universidad Ciclo del Azufre [ Características ] Etapas e Importancia en 2022 Trucos para la universidad](https://i.pinimg.com/originals/ff/7d/40/ff7d40d216804c28456d84ad061651ee.png)
Ciclo del Azufre [ Características ] Etapas e Importancia en 2022 Trucos para la universidad

Diagrama De Punto De Lewis Azufre

7. Unidad TRES Determinación del punto de fusión y ebullición Determinación del punto de

Características del azufre Explora Univision

Azufre Tabla periodica

Punto de ebullición. Lección teórica. YouTube
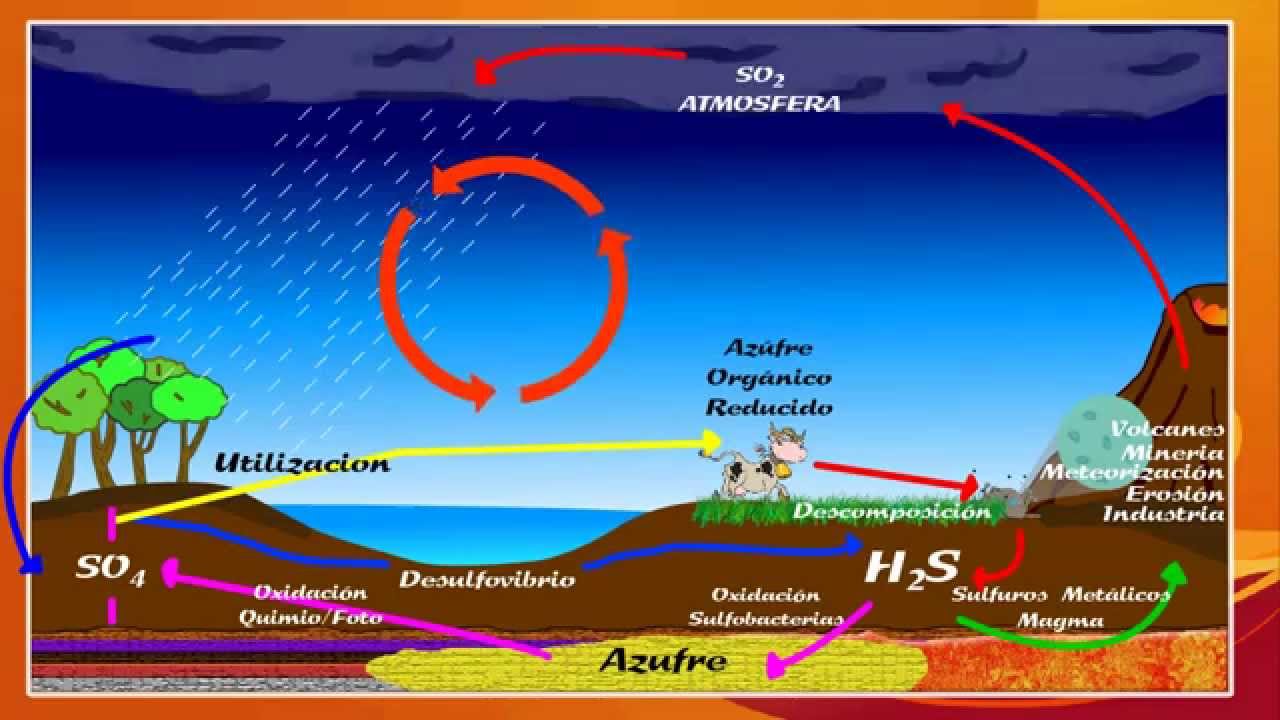
Esquema del ciclo del azufre ¡Fotos & Guía 2021!
![🌡 Puntos de Fusión y Ebullición 🔥 ¿Qué son? EJEMPLOS [Fácil y Rápido] FÍSICA QUÍMICA YouTube 🌡 Puntos de Fusión y Ebullición 🔥 ¿Qué son? EJEMPLOS [Fácil y Rápido] FÍSICA QUÍMICA YouTube](https://i.ytimg.com/vi/6WN6TFo9TfE/maxresdefault.jpg)
🌡 Puntos de Fusión y Ebullición 🔥 ¿Qué son? EJEMPLOS [Fácil y Rápido] FÍSICA QUÍMICA YouTube

PPT punto de ebullición PowerPoint Presentation, free download ID3116840

¿Qué es el dióxido de azufre y cuáles son sus consecuencias? Hidrolab
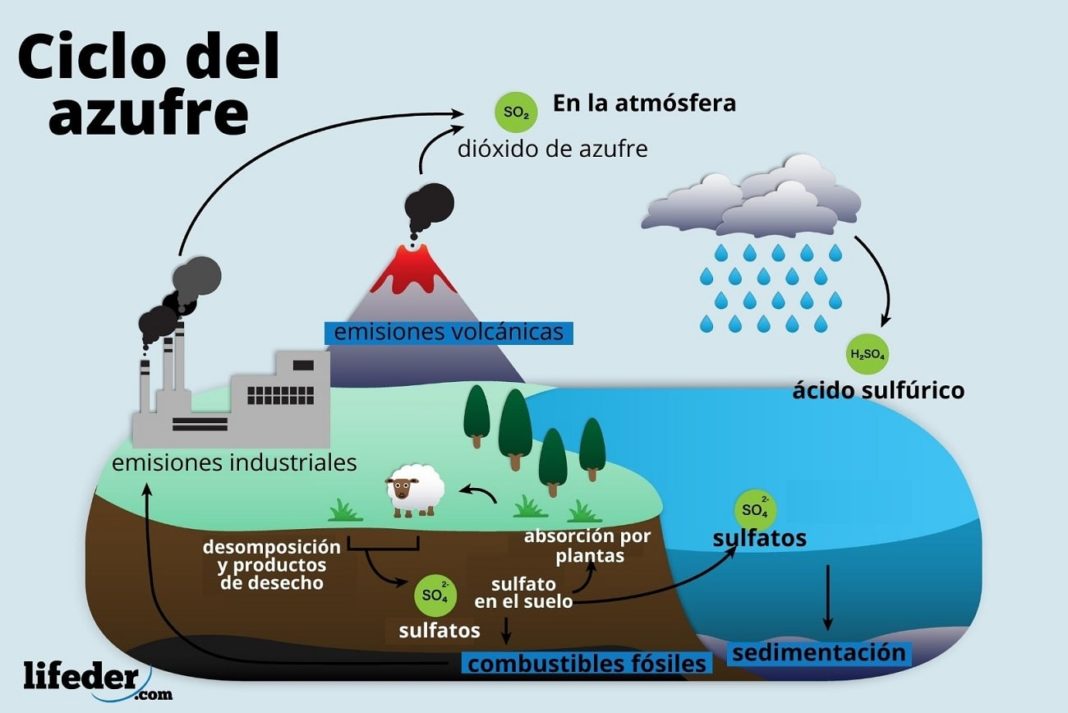
Ciclo del azufre características, etapas, importancia
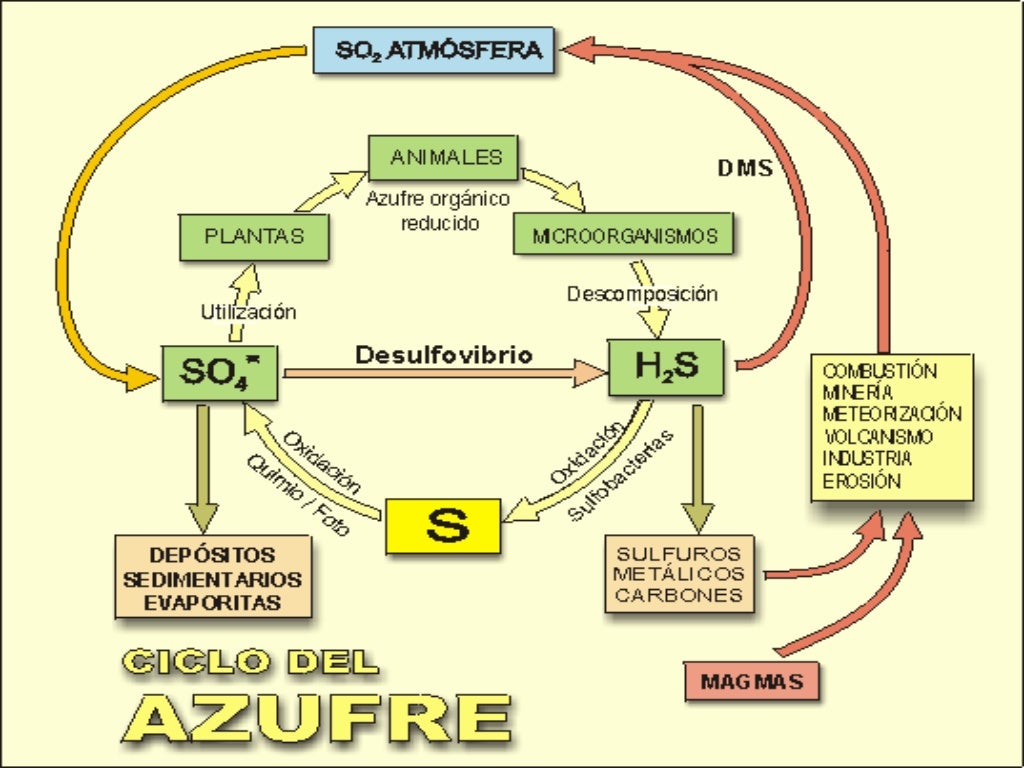
Ciclo de azufre
El azufre es un elemento no metálico que lidera, por debajo del oxígeno, el grupo de los calcógenos de la tabla periódica. Se ubica específicamente en el grupo 16 con período 3, y su símbolo químico es S. De sus isótopos naturales, el 32 S es por mucho el más abundante (alrededor del 94% de todos los átomos de azufre).. El azufre es un elemento químico de número atómico 16 y símbolo S (del latín sulphur).Es un no metal abundante con un color amarillo característico. [1] Dicho elemento es generado en estrellas masivas en las que predominan temperaturas que provocan la fusión entre un núcleo de silicio y otro de helio en un proceso denominado nucleosíntesis de supernovas.