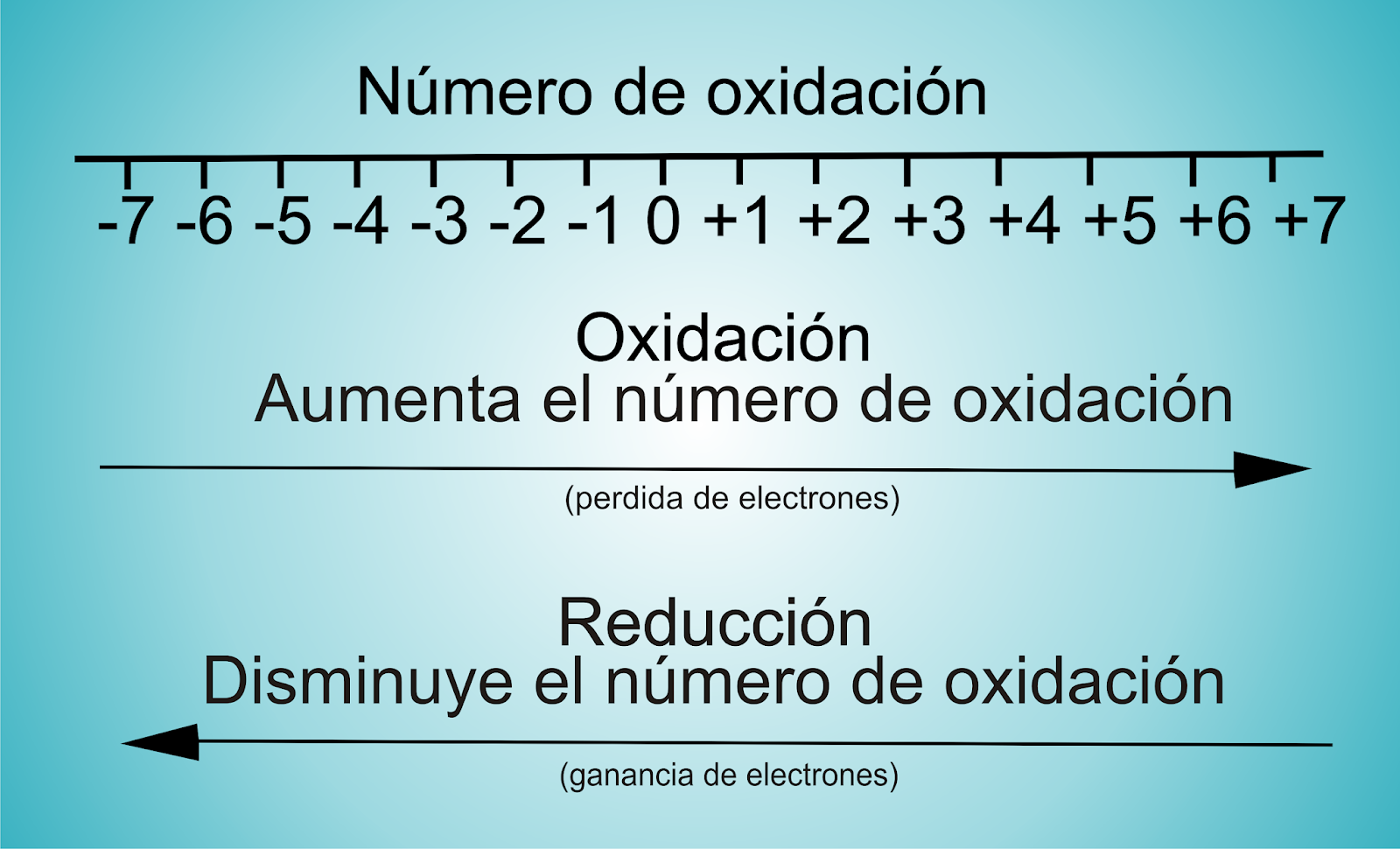
En química se llama oxidación al fenómeno químico en el que un átomo, molécula o ión pierde uno o varios electrones, aumentando así su carga positiva. Como el oxígeno es un elemento que usualmente acepta dichos electrones, se llamó a este tipo de reacciones, reacciones de reducción-oxidación, reacciones de óxido-reducción o.. Regla 2: el número de oxidación de un ion es el mismo que su carga. Un ion es un átomo con carga debido a la ganancia o pérdida de electrones. La carga se indica como superíndice después del átomo. Si un átomo tiene esto, significa que es un ion. Por ejemplo, el ion potasio tiene una carga +1, por lo que el número de oxidación es +1.

numero de oxidacion de los elementos de la tabla periodica Brainly.lat
TERCER PERIODO ACADÉMICO Ciencias Naturales

Ejemplos De Numeros De Oxidacion Images and Photos finder

Redox. Cálculo del número de oxidación YouTube

Determinación del número de oxidación YouTube

Numero De Oxidacion Acido

¿Qué es el número de Oxidación? YouTube

Números de oxidación (estados de oxidación) YouTube

Números de oxidación y enlaces químicos
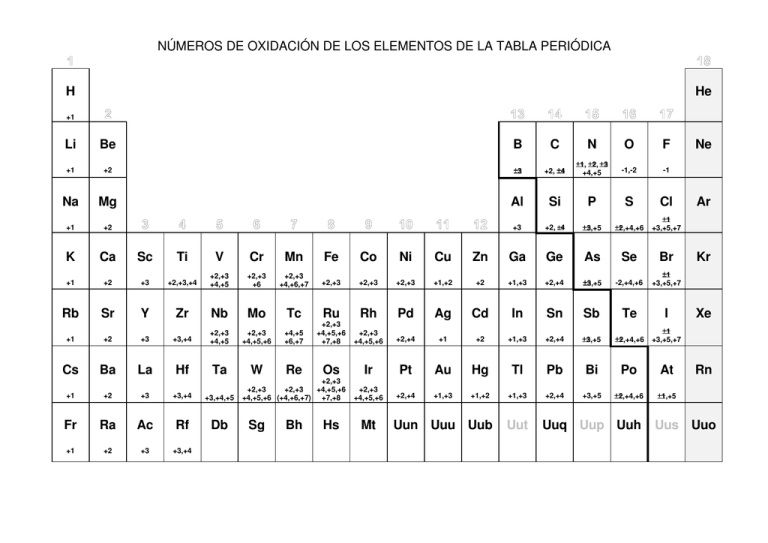
NÚMEROS DE OXIDACIÓN DE LOS ELEMENTOS DE LA TABLA
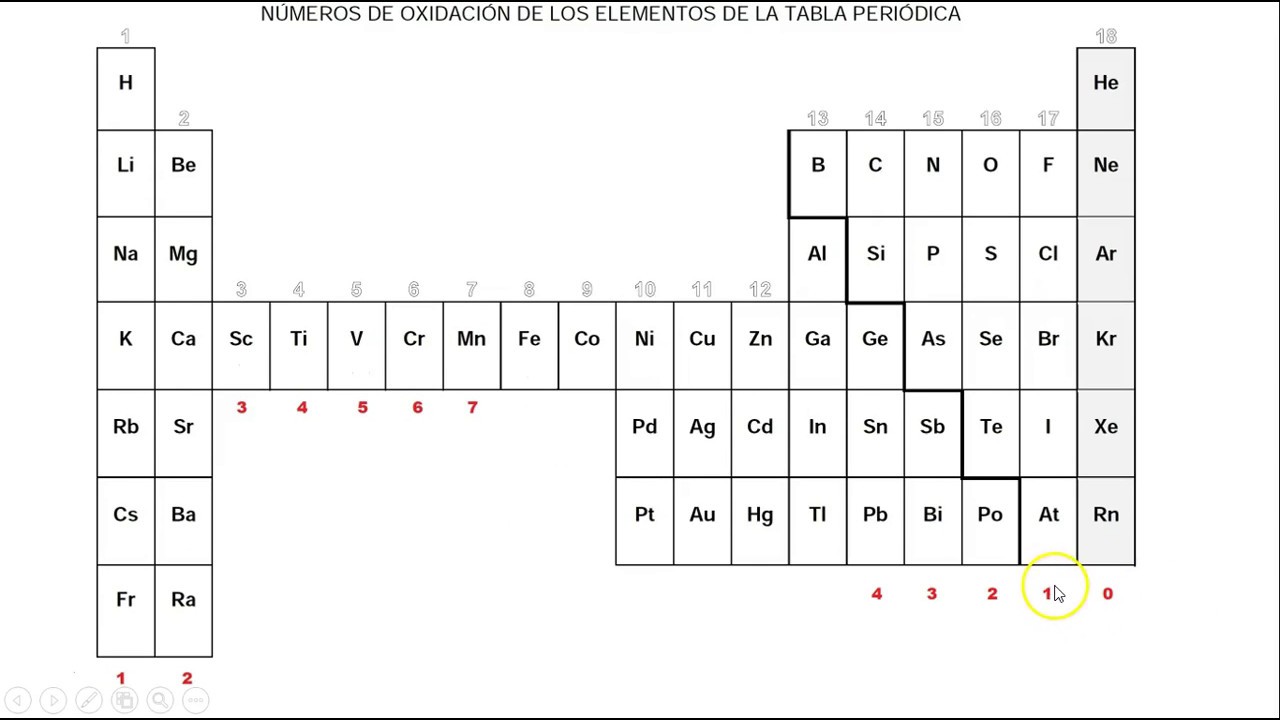
APRENDER LOS NÚMEROS DE OXIDACIÓN FÁCILMENTE YouTube
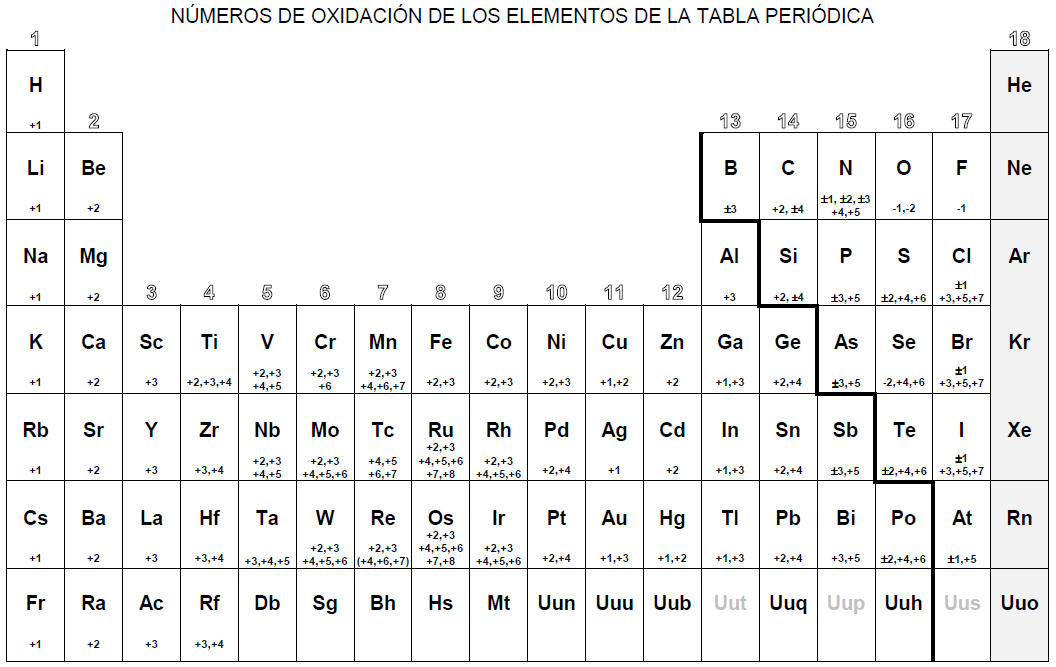
numero de oxidacion

Estados De Oxidacion De Los Elementos

Aprende las VALENCIAS o NÚMEROS DE OXIDACIÓN en menos de 10 MINUTOS YouTube
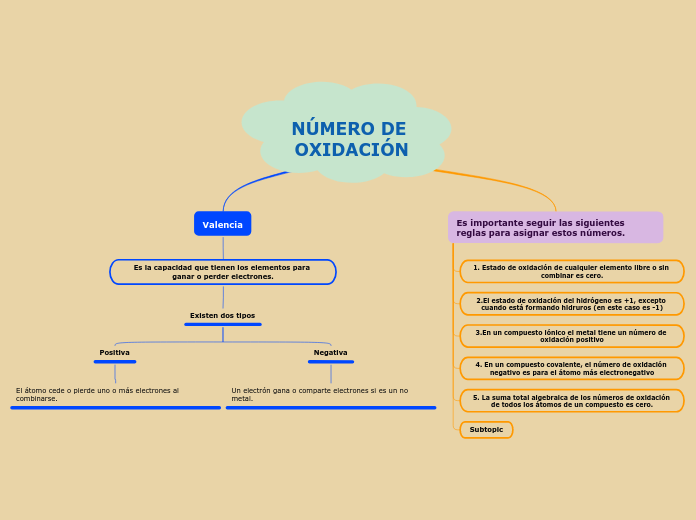
NÚMERO DE OXIDACIÓN Mind Map

Asignación del número de oxidación de un elemento en un compuesto YouTube

Calculo de Número de Oxidación de un Compuesto. FÁCIL. YouTube

Quimica 2.2.5 Número de oxidación.

Como encontrar el número de oxidación de un compuesto YouTube
![⚠️Número de oxidación Estados de oxidación EJERCICIOS⚠️ [Fácil y Rápido] QUÍMICA YouTube ⚠️Número de oxidación Estados de oxidación EJERCICIOS⚠️ [Fácil y Rápido] QUÍMICA YouTube](https://i.ytimg.com/vi/qXnL4mLfeV4/maxresdefault.jpg)
⚠️Número de oxidación Estados de oxidación EJERCICIOS⚠️ [Fácil y Rápido] QUÍMICA YouTube
a) Los números de oxidación apropiados son. Los únicos átomos que cambian son Mn, de +7 a +2, una reducción, y S, de +4 a +6, una oxidación. La reacción es un proceso redox. SO 2 ha sido oxidado por MnO 4 —, y entonces MnO 4 — es el agente oxidante. MnO 4 — se ha reducido en SO 2, y así SO 2 es el agente reductor.. En estos casos, el número de oxidación es -1 para los halógenos y -2 para el oxígeno. – En una molécula o ion poliatómico, la suma de los números de oxidación de todos los átomos debe ser igual a la carga total del molécula o ion. Siguiendo estas reglas, podemos calcular el número de oxidación de un átomo en una molécula o ion.